2018年12月5日,刚刚,国家药品监督管理局发布广州白云山天心制药股份有限公司等6家药企跟踪检查通报,收回5家企业GMP证书,1家由于长期停产责令进行整改。

上海安丁生物(汤阴) 药业有限公司
检查发现问题:根据国家药品监督管理局药品跟踪检查计划,核查中心组织对上海安丁生物( 汤阴) 药业有限公司的氨咖黄敏胶囊、氨酚咖敏颗粒开展现场检查。检查发现该公司主要存在以下问题:
一、未完全按《药品补充申请批件》要求完成有关工作。
该公司共有93个批准文号,分别在2014年至2015年期间完成了变更企业名称及变更药品生产场地的补充申请,取得了《药品补充申请批件》(批件号:豫B201500089、豫B201401532等),批件中要求品种在新地址生产时,前三批样品须经安阳市食品药品监督管理局现场核查并抽样,安阳市食品药品检验所检验合格后,由安阳市食品药品监督管理局批准上市销售。企业至今已生产了23个品种25个品规并上市销售,但取得安阳市食品药品监督管理局同意上市销售函的有12个品种13个品规,其余11个品种12个品规均为获得上市销售函。
二、企业未对质量风险进行评估和调查。
(一)氨咖黄敏胶囊(批号:161001,理论批量:350万粒)批生产记录显示:2016年10月4日企业将不同时间生产的小试、中试和大生产产品在总混工序进行了混合、中间品检验、内包、外包、入库,现已销售完毕。企业仅对该批产品进行了检验,对该批产品的生产过程、质量可控性、中间品储存过程控制以及是否符合相关法规要求未进行任何风险评估即予放行。
(二)氨咖黄敏胶囊(批号:161001,理论批量:350万粒)产品中试过程中,原料咖啡因的投料量计算有误;成品检验报告中咖啡因的含量为107.1%,而企业规定的内控标准含咖啡因应为标示量的93.0%-107.0%(法定标准含咖啡因应为标示量的90.0%-110.0%),企业未按偏差程序进行调查,也未进行相应风险评估。
(三)企业2016年8月在生产线上新增氨咖黄敏胶囊生产,未进行交叉污染的风险评估。
三、实验室数据管理不规范。
(一)实验室未按照企业制定的《实验室原始数据的管理规定》对薄层色谱照片进行电子数据管理,仅由实验员手机拍照后打印,原始电子照片未进行统一存储和备份。
(二)实验室大型精密仪器未达到三级权限管理要求:HPLC、GC、IR和AAS等仪器的计算机windows系统登录均未设置分级权限,实验室QC主管xxx为HPLC、GC、AAS计算机管理员,采购部人员xxx为IR计算机管理员,且windows的删除权限未被禁止,仅禁止了时间修改功能。实验室检验员均使用计算机管理员帐户进行仪器操作。
(三)HPLC(编号:JY-014)计算机中存在部分难以溯源文件,如存储通道为G盘新建文件夹201文件夹中记录有2016.3.4的进样数据(包括氨基比林对照1、2,咖啡因,溶剂,样1-2),提示为酚氨咖敏颗粒,但电子数据无样品名称、批号等信息,且追溯仪器使用记录未见登记、未出报告;如存储通道为G盘成品半成品酚氨咖敏颗粒1600302成品马来酸氯苯那敏的文件夹中包含“新建文件夹”,其中有文件名为“样1-1,样1-2,样1-3,样1-4”的数据,且追溯仪器使用记录未见登记、未出报告。
四、对照品管理不规范。
(一)酚氨咖敏颗粒成品检验中,咖啡因含量测定所用对照品为该企业生产所购的咖啡因原料。该原料作为工作对照品使用时未进行标定,并用于9批产品(160301-04,160901-05)的放行检验。
(二)9批(160301-04,160901-05)酚氨咖敏颗粒成品放行检验中,马来酸氯苯那敏含量测定均采用100047-200606批对照品已过期,但未对过期对照品的特性量值及适用性进行验证便用于产品放行检验。
(三)酚氨咖敏颗粒处方中的辅料蔗糖红外鉴别项目中,蔗糖对照品(批号:111507-20001)仅于2015年5月11日扫描一次,用于2015年-2017年36批蔗糖样品的红外图谱进行对比,且标准品、对照品领用台账中无相关对照品领用记录。
(四)对照品入库台账显示100334-201803批双氯芬酸钠对照品库存10瓶(2018年5月6日购入5瓶,2018年7月15日购入5瓶),现场库存5瓶,查询对照品领用台账未见其领用记录。
处理措施:该企业质量管理体系不能有效运行,在注册要求符合性、质量风险管理、数据可靠性、质量控制与质量保证等方面存在严重问题,其氨咖黄敏胶囊、酚氨咖敏颗粒的生产质量管理不符合《药品生产质量管理规范(2010年修订)》相关规定,责成河南省药品监督管理局收回该企业相关药品GMP证书,并依法调查处理。
贵州德良方佰仕特药业有限责任公司
根据国家药品监督管理局药品跟踪检查计划,核查中心组织对贵州德良方佰仕特药业有限责任公司开展现场检查。检查发现该公司主要存在以下问题:
一、特药安全管理不符合特殊药品法规要求。
二、质量控制实验室管理不规范。
(一)一原料紫外鉴别无谱图,无样品配制记录,企业配备的紫外分光光度计不支持图谱导出或打印,无使用前仪器的校正检查的规定和记录。
(二)HPLC测定未做系统适用性试验,SOP中亦未规定。
(三)含量测定有手动积分情形,无相应的审批记录,检验SOP中未对积分事件作出规定。
三、计算机化系统不符合要求。
(一)紫外分光光度计、高效液相色谱仪、气相色谱仪、原子吸收分光光度计等均为单机版,均未配备审计追踪功能。
(二)高效液相色谱仪色谱工作站是N2000,版本号是4.0,无账户登录和分级权限控制,电脑系统未禁止剪切、删除、重命名等功能,系统时间亦未锁定。
(三)电脑系统无QA人员登录账号。
四、在机构与人员、确认与验证、委托生产方面还存在一般缺陷3条。
处理措施:该公司在特药安全管理方面、质量控制实验室管理方面存在严重问题,鉴于企业处于长期停产状态,责成贵州省药品监督管理局监督企业在整改完成前不得恢复生产。
贵州德良方药业股份有限责任公司
检查发现问题:根据国家药品监督管理局药品跟踪检查计划,核查中心组织对贵州德良方药业股份有限责任公司的消炎止咳胶囊委托生产情况进行现场延伸检查。检查发现该公司主要存在以下问题:
一、特药安全管理不符合特殊药品法规要求。
二、计算机化系统不符合要求。
(一)紫外分光光度计、高效液相色谱仪、气相色谱仪、原子吸收分光光度计等均为单机版,均未配备审计追踪功能。
(二)高效液相色谱仪色谱工作站是N2000,版本号是4.0,无账户登录和分级权限控制,电脑系统未禁止剪切、删除、重命名等功能,系统时间亦未锁定。
(三)电脑系统无QA人员登录账号。
三、质量控制与质量保证不符合要求。
(一)一原料紫外鉴别无谱图,无样品配制记录,企业配备的紫外分光光度计不支持图谱导出或打印,无使用前仪器的校正检查的规定和记录。
(二)HPLC测定未做系统适用性试验,SOP中亦未规定。
(三)含量测定有手动积分情形,无相应的审批记录,检验SOP中未对积分事件作出规定。
(四)该企业现行的检验操作SOP大多为2013年生效执行,企业未按照2015年版药典要求进行升级修订,亦未开展相应的人员培训;企业实际检验操作按照SOP执行,现场交流发现检验人员对2015年版药典的要求不熟悉。
(五)高温设备使用日志内容不全,未体现器皿恒重、对照品干燥等信息。
(六)实验室未建立样品接收、分样、领用、暂存记录,对罂粟壳、麻黄在实验室中的粉碎、剩余样品、废弃处理未建立记录。
(七)未建立高效液相色谱仪、气相色谱仪维护记录,现场询问实验室人员,高效液相色谱仪(手动进样)的进针垫片一直未更换,气相色谱仪衬管一直未更换;未建立色谱柱保养记录;智能崩解仪未按药典要求进行校准;双量程电子天平未配备十万分之一精度所要求的E2级标准砝码。
(八)稳定性考察样品在普通留样室中存放,未放置在考察箱中,不符合药典要求。
(九)2017年度消炎止咳胶囊回顾分析报告内容不全,缺少稳定性考察情况等内容;对数据趋势未运用统计学方法进行分析;对报告中表述的总收率波动较大的情况未开展相应的调查处理。
(十)该企业2015年至今无偏差、OOS、CAPA报告情况。检查组在检查过程中发现企业在多方面存在问题,如标准管理、记录管理等明显的偏差,显示企业在异常情况发现、处理等方面存在问题。
四、确认与验证存在问题。
(一)胶囊剂生产线对自有品种柏花草胶囊、灵芝胶囊进行了清洁验证;在增加委托生产品种后,仅对共用可行性开展了评估,未考虑罂粟壳、麻黄的属性及可能带来的交叉污染风险,未开展相应的风险评估及清洁验证;未采取相应的控制措施如阶段性生产或指定特殊药品专用生产设备等。
(二)消炎止咳胶囊现行工艺规程中对直接入药的生粉规定进行灭菌,灭菌方法有两种:CO60幅照灭菌和湿热灭菌。企业进行了湿热灭菌方式的工艺验证,但未对灭菌方式是否对产品质量造成影响开展评估,未根据验证开展情况对工艺规程进行修订。
五、数据可靠性问题。
显微鉴别原始记录只有文字表述,无照片、影像或描图数据,现场未发现水合氯醛,企业亦提供不出配制记录,未配备检验样品对应的显微图谱,实验人员未开展显微鉴别培训,现场询问实验人员不能回答实验操作要求,企业无法证明实际开展了显微鉴别实验。中检院穿心莲对照药材现批号为121082-201505,而企业批号为121082-200302。
六、在机构与人员、设备、生产管理还存在一般缺陷3项。
处理措施:该公司在特药安全管理方面不符合法规要求,质量管理体系不能有效运行,在质量控制与质量保证、计算机化系统、确认与验证、数据可靠性等方面存在严重问题,其消炎止咳胶囊生产质量管理不符合《药品生产质量管理规范(2010年修订)》要求。责成贵州省药品监督管理局收回该企业相关药品GMP证书,并进一步调查处理。
广州白云山天心制药股份有限公司
检查发现问题:根据国家药品监督管理局药品跟踪检查计划,核查中心组织对广州白云山天心制药股份有限公司的注射用盐酸头孢甲肟开展现场检查。检查发现该公司主要存在以下问题:
一、直接接触药品的容器未经批准、未验证用于部分批次的产品生产。检查期间,该公司已启动召回程序,对两批产品进行召回。
二、企业对产品的特性研究不充分、数据分析不全面,对注射用盐酸头孢甲肟的生产质量的管理不完善。
(一)现场检查时,注射用盐酸头孢甲肟(规格:1.0g,批号:180856)的包装工序未监测光照强度、温度等产品影响因素。180301批批记录显示注射用盐酸头孢甲肟(规格:1.0g)分装、轧盖操作结束时,未记录温、湿度。
(二)盐酸头孢甲肟与无水碳酸钠混合验证时,仅提供了两批产品(180301、180302)的验证数据,且无不同时间点、不同取样点的描述,对数据分析不全面。
(三)注射用水日常记录的数据与仪器监测的数据出现偏离未及时调查原因。
(四)盐酸头孢甲肟采用西林瓶包装留样,与市售包装不一致,也未采用模拟包装。
(五)企业变更管理台账中,对变更原辅料供应商等重要变更等级均评定为中度变更,与制定的变更管理规程不一致。
(六)2018年8月2日培训检验员使用了一瓶180302批注射用盐酸头孢甲肟,无取样记录。
(七)质量部的个别取样员未经取样相关培训;碳酸钠含量检测原始记录无计算公式,直接由电脑计算,无法体现修约规则,易产生误差。
(八)部分检验项目原始记录未代入滴定液校正值进行计算,例如低硼硅玻璃管制注射剂瓶(20180143批)内表面耐水性检测未将0.01mol/L的盐酸滴定液校正值代入计算。
三、部分工序未按要求对洁净区的悬浮粒子进行动态监测。
混粉工序操作人员需进入B级背景下的A级层流罩下进行称量、混粉操作,对无菌药粉的暴露工序存在潜在的污染风险;头孢粉针大楼5层的监控室里的监控系统显示该楼4层的混粉(静态)、分装(动态)等工序无菌生产过程时,B/A区尘埃粒子的数据均为0。
处理措施:该企业注射用盐酸头孢甲肟的生产质量管理不符合《药品生产质量管理规范(2010年修订)》相关规定,责成广东省药品监督管理局收回该企业相关药品GMP证书,并进一步调查处理。
比智高药业有限公司
检查发现问题:根据国家药品监督管理局药品跟踪检查计划,核查中心组织对比智高药业有限公司的解郁安神颗粒开展现场检查。检查发现该公司主要存在以下问题:
一、工艺验证。
(一)工艺再验证(批号:20130902、20140201、20140202)产品未进行质量评估和稳定性考察,企业整改仅对相关人员进行了《留样管理规程》和《产品持续稳定性考察管理规程》的培训和考核。解郁安神颗粒原批量为10万袋,企业进行了工艺再验证(批号:20130902、20140201、20140202),于2015年7月变更批量为20万袋。上述三批产品未进行质量评估和稳定性考察,不足以支持进行批量变更。
(二)未对解郁安神颗粒干膏粉的贮存时限(企业规定贮存期6个月,复验后可再贮存6个月)进行验证。企业整改仅对历史检验记录数据的水分、微生物进行回顾分析,未制定干膏粉贮存时限验证方案进一步对干膏粉有效指标(如含量)进行考察。
二、数据管理和文件记录。
(一)液相色谱仪(SH-10-03)工作电脑的回收站中发现有2018年5月25日删除的2014年3月的栀子检验系统适用性试验数据。企业整改未针对防止删除数据问题再次发生采取预防措施。
(二)QC实验室检验台账、取样台账,QA变更台账、偏差台账均为Word格式的电子版本,储存上述台账的电脑无权限管理设置。经现场核对,中药材检验台账中部分批次检验结果项目为空白,检验台账中部分中药材批次信息与原辅料台账中的相应信息不一致。
三、中药饮片炮制。未制定中药饮片的炮制规程、批量范围,制远志(批号:J160101,批量179.6kg;J160102,批量19.6 kg)生产记录中显示干燥、煎煮、辅料计算均与药典要求不一致。企业整改已制订了远志、柴胡、酸枣仁、甘草等药材的饮片炮制规程,炮制方法与中国药典2015年版一致,计划后期做三批炮制药材的工艺验证,但未完全落实。
处理措施:该企业对上述工艺验证、数据管理和文件记录为主要缺陷的问题,未整改到位或未采取适当的预防措施防止此类缺陷再次发生,其解郁安神颗粒的生产质量管理不符合《药品生产质量管理规范(2010年修订》相关规定,责成吉林省药品监督管理局收回该企业相关药品GMP证书,并进一步调查处理。
江苏七0七天然制药有限公司
检查发现问题:根据国家药品监督管理局药品跟踪检查计划,核查中心组织对江苏七0七天然制药有限公司的的沉香化气丸开展现场检查。检查发现该公司主要存在以下问题:
一、物料管理不规范,部分无标识,无法确保物料防止污染和正确的储存、运发
(一)洁净区原辅料暂存间供制粒用乙醇(批号F-0600-1801)和一般区制粒用乙醇(批号F-0600-1802)已被污染,塑料桶(外标识为“提取”)内有黑色异物,其中一桶密封不严;
(二)玉米淀粉、乙醇等已入洁净区暂存间台账的物料,尚存在一般区电梯口,未受控管理;
(三)金胆片工艺规程(TS-SC-001-17)中明确其中间产品(总混颗粒)应冷处存放(2-8℃),但因冷库面积不够,4批颗粒(批号180511、180512、180513、180514)存放于洁净区中转站,房间控制温度为18-26℃;
(四)金胆片素片(批号:180506)存放时间(2018-5-23至2018-5-29)超过工艺规程中的最长贮存时间(3天);
(五)中间站中金胆片素片(180507)共12袋,其中6袋进行了标识,其余6袋未进行标识。
二、不能有效防止生产操作过程的混淆
生产操作过程发生混批。检查期间,生产操作岗位人员及QA生产前没有正确核对中间产品信息,导致生产过程发生差错,5月25日在固体制剂车间洁净区金胆片(批号:180505)塑瓶分装工序有1桶金胆片糖衣片(批号180504,81kg)混入。
三、部分偏差未开展偏差调查
(一)个别药材检验出现OOS,未及时进行调查即进行复检,如:砂仁(批号Y-1151-1501)含量检测未进行系统适应性试验,2015年5月6日第一次检测不合格,未进行调查处理即复检,复检合格后放行;
(二)沉香化气丸(批号150701)批生产记录中显示其混合粉存放时限为50天(2015.5.18-2015.7.8),超过其规定的30天,企业未进行偏差调查和处理。
处理措施:该企业未明确药材微生物的控制方式,在物料管理、生产管理、偏差调查等方面存在严重问题,其沉香化气丸的生产质量管理不符合《药品生产质量管理规范(2010年修订)》相关规定,责成江苏省药品监督管理局收回该企业相关药品GMP证书,并进一步调查处理。
▌12月5日,广东省药监局发布2018年第5号收回药品GMP证书公告。
广东清源中药饮片有限公司、化州市光华中药饮片有限公司、广州南北行中药饮片有限公司、惠州市东华中药饮片有限公司4家药企不符合《药品生产质量管理规范》,依据《药品生产质量管理规范认证管理办法》第三十三条规定,该局依法收回其《药品GMP证书》。这4张GMP证书的认证范围均是中药饮片。
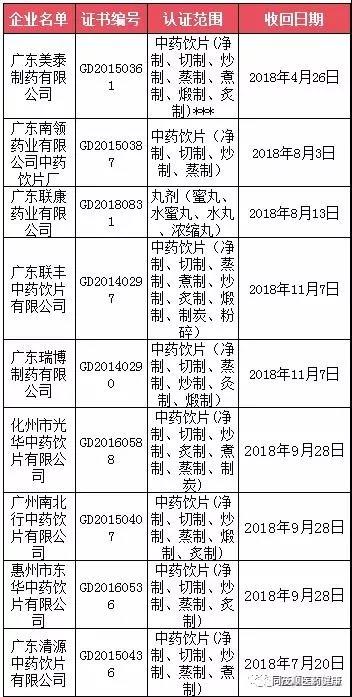
据统计,2018年广东省药监局共收回9家药品生产企业的GMP证书,除上述4家企业外,还包括广东美泰制药有限公司、广东南领药业有限公司中药饮片厂、广东联康药业有限公司、广东联丰中药饮片有限公司、广东瑞博制药有限公司。
从认证范围来看,除了一张为丸剂外,其余8张均是中药饮片。